Anilin
[2]Anilin (aminobenzol, fenilamin) – C6H5NH2 formulasına malik olan üzvi birləşmədir, sadə aromatik amindir.
| Anilin | |
|---|---|
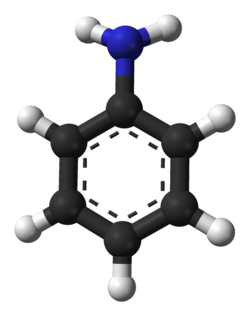 | |
| Ümumi | |
| Kimyəvi formulu | C6H5NH2 |
| Molyar kütlə | 93.1265 q/mol |
| Fiziki xassələri | |
| Sıxlıq | 0,8786 q/sm³ |
| Termik xüsusiyyətlər | |
| Ərimə nöqtəsi | 6.3 °S |
| Qaynama nöqtəsi | 184.13 °S |
| Öz-özünə yanma temperaturu | 615 ± 1 °C[1] |
| Buxarın təzyiqi | 0,6 ± 0,1 mm Hg |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 62-53-3 |
| PubChem | 6115 |
| RTECS | BW6650000 |
| ChEBI | 17296 |
| BMT nömrəsi | 1547 |
| ChemSpider | 5889 |
Ümumi məlumat
redaktəRəngsiz, yağa bənzər maye olub xarakterik iyə malikdir. Suda yaxşı həll olmur, üzvi həlledicilərdə yaxşı həll olur. Havada tez oksidləşərək tünd qırmızı rəng alır. Zəhərlidir. “ Anilin “ sözü tərkibi “ İndigofera anil “ adlı bitkidən götürülüb (bitkinin müasir beynəlxalq adı “ İndigofera suffruticosa “-dır).
Tarixi
redaktə- Anilin ilk dəfə 1826-cı ildə alman kimyaçısı Otto Unferdorben tərəfindən indiqo ilə əhəngin qovulmasından alınmışdır ki, o da ona “ kristalin “ adını vermişdir.
- 1834-cü ildə Fridlib Ferdinand Runge daş kömür qətranında anilini kəşf edib və “ kianol “ adlandırıb.
- 1840-cı ildə Yuliy Fritsşe indiqo ilə KOH məhlulunu qızdırmaqla anilin almışdır və “ anilin “ adlandırmışdır.
- 1841-ci ildə Nikilay Zinin nitrobenzolu (NH4)2S təsirində reduksiya etməklə anilin almışdır və onu “ benzidam “ adlandırmışdır.
Alınması
redaktəSənayedə anilini 2 mərhələdə alırlar. Birinci mərhələdə benzolu qatı nitrat və sulfat turşusu ilə 50-600 C temperaturda nitrolaşdırırlar, nəticədə nitrobenzol əmələ gəlir. İkinci mərhələdə nitrobenzolu katalizator iştirakında 200-3000 C temperaturunda hidrogenləşdirirlər :
- C6H5NO2 + 3H2 → C6H5NH2 + 3H2O
İlk dəfə nitrobenzolun reduksiyası dəmir ilə aparılmışdır :
- 4C6H5NO2 + 9Fe + 4 H2O → 4C6H5NH2 + 3Fe3O4
Başqa üsulla anilini nitrobirləşmələri reduksiya etməklə alırlar- Zinin reaksiyası :
- C6H5NO2 + 3(NH4)2S → C6H5NH2 + 6NH3 + 3S + 2H2O
Kimyəvi xassələri
redaktəAnilin üçün həm amin qrupunda, həm də aromatik halqada reaksiyalar xarakterikdir. Bir tərəfdən benzol halqası amin qrupunun əsası xassəsini alifatik aminlərə və hətta ammonyaka nisbətən zəiflədir. Digər tərəfdən aminqruplarının təsirindən benzol halqası əvəzetmə reaksiyalarına benzola nisbətən daha aktiv daxil olur. Yaxşı halogenləşir, nitrolaşır və sulfolaşır.
Oksidləşməsi
redaktə[3]Alifatik aminlərdən fərqli olaraq, aromatik aminlər asanlıqla oksidləşirlər. Buna misal olaraq xrom qarışığının anilinlə reaksiyasını göstərmək olar. Bu reaksiya nəticəsində “ qara anilin “ boyağı alınır.
Azotla reaksiyası
redaktəNitrit turşusu ilə anilin diazonium kationu əmələ gətirir :
- C6H5NH2 +NaNO2 + 2HCl → C6H5N+2Cl- + NaCl + 2H2O
Bu reaksiyadan fenolun alınmasında istifadə olunur. Ancaq xlorid turşusu əvəzinə durulaşdırılmış sulfat turşusu götürülməlidir :
- 2 C6H5NH2 +2NaNO2 + 2H2SO4 → (C6H5N+2)2 SO4 + Na2SO4 + 4H2O → 2 C6H5OH + 2N2 ↑ + Na2SO4 + H2SO4 + 2H2O
Başqa reaksiyalar
redaktə[4]Anilinin xlorid turşusu ilə qarşılıqlı təsirindən fenilammonium xlorid alınır :
- C6H5NH2 + HCl → [C6H5NH3]Cl
İstehsalı və tətbiqi
redaktə[5]Əvəllər anilini nitrobenzolu molekulyar hidrogenlə reduksiya etməklə alırdılar ki, nəticədə çıxım 15%-dən çox olmurdu. Qatılaşdırılmış xlorid turşusunun dəmirlə qarşılıqlı təsirindən alınan atomar hidrogen molekulyar hidrogendən aktiv olduğuna görə Zinin reaksiyası anilin alınmasında daha əlverişli üsuldur. Burada nitrobenzol anilinə reduksiya edilir. Anilindən həm də süni kauçuk istehsalında da istifadə edilir.
Zəhərli xassələri
redaktəAnilin mərkəzi əsəb sisteminə neqativ təsir göstərir. Anilinin buxarları orqanizmə tənəffüs yolları ilə, hətta dəri vasitəsilə də keçə bilər. Anilinlə zəhərləndikdə zəiflik, baş gicəllənmə, baş ağrıları, dodaqların göyərməsi müşahidə olunur. Bundan əlavə ürəkbulanma, qusma da olur. Anilinlə xroniki zəhərlənmədən toksiki hepatit və psixi-əsəb pozuntuları baş verir.
Ədəbiyyat
redaktə- Артеменко А. И. Органическая химия. — М.: «Высшая школа», 1987. — 430 с.
İstinadlar
redaktə- Анилин// Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Анилиновое отравление // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
Qeyd
redaktə- ↑ http://www.cdc.gov/niosh/ipcsneng/neng0011.html.
- ↑ ↑ Перейти к:1 2 3 4 5 6 7 8 http://www.cdc.gov/niosh/npg/npgd0033.html Arxivləşdirilib 2022-04-18 at the Wayback Machine
- ↑ Окисление анилина раствором хлорной извести. Единая коллекция цифровых образовательных ресурсов. Проверено 14 августа 2017.
- ↑ Цветков Л.А. § 36. Амины // Органическая химия. Учебник для 10 класса. — 20-е изд. — М.: Просвещение, 1981. — С. 171—175.
- ↑ Aniline (англ.) (недоступная ссылка — история). www.the-innovation-group.com (19 February 2002). — Aniline producers price capacity market demand consumption production growth uses outlook n.d., The Chemical Market Reporter, Schnell Publishing Company. Проверено 14 августа 2017. Архивировано 19 февраля 2002 года.