Xloroform
Xloroform (Trixlormetan, metiltrixlorid, xladon20) — üzvi kimyəvi birləşmə. Kimyəvi formulu CHCl3. Adi şəritdə efir iyinə oxşar iyə malikdir, rəngsiz uçucu mayedir və şirin dadı var. Praktiki olaraq suda həll olmur, su ilə kütlə həcmində 0,23% miqdara kimi qarışa bilir. Bütün üzvi həlledicilərdə həll olur və yanmır. Günəş işığında isti şəraitdə çox qaldıqda fosgenlə zəhərlənmə verir.
| Xloroform | |
|---|---|
 | |
 | |
| Ümumi | |
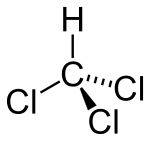
| Kimyəvi formulu | CHCl3 |
| Molyar kütlə | 119,38 q/mol |
| Fiziki xassələri | |
| Sıxlıq | 1,483 q/sm³ |
| Termik xüsusiyyətlər | |
| Ərimə nöqtəsi | −63,5 °S |
| Qaynama nöqtəsi | 61,2 °S |
| Buxarın təzyiqi | 160 ± 1 mm Hg[1] |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 67-66-3 |
| PubChem | 6212 |
| RTECS | FS9100000 |
| ChEBI | 35255 |
| ChemSpider | 5977 |
Tarix
redaktəXloroform ilk dəfə 1831-ci ildə kauçukun həlledicisi kimi biri birindən asılı olmayaraq Samuel Qutri (Samuel Guthrie) sonra isə Libix Justis (Justus von Liebig) və Subereyn (Eugène Soubeiran) tərəfindən alınıb. Xloroform formulası fransız kimyaçısı Jan-Batist Düma tərəfindən müəyyən edilib. O 1834-cü ildə xloroform adını düşünüb vermişdir. Bu birləşmə hidroliz olunduqda qarışqa turşusunu əmələ gətirir.
Kliniki praktikada ümumi anestezisiyaedici maddə kimi ilk dəfə 1847-ci ildə Holmos Kut (Holmes Coote) istifadə etmişdir. O, tibb işcisi Jeyms Simpson tərəfindən geniş formada istifadə olunmuşdur. Xloroformdan doğuş zamanı ağrıları azaltmaq üçün istifadə edilmişdir.
Rusiyada tibbi xloroform istehsalını 1916-cı ildə Boris Zabarski təklif etmişdir. Həmin vaxtlarda o, Uralda Perm vilayətinin Vsevolodo-Vilva kəndində yaşayırmış.
Fiziki xassələri
redaktə- Şuasındırma əmsalı: 1,44858 15 °C.
- Kristallaşma temperaturu: −63,55 °C
- Qaynama temperaturu: 61,152 °C
- Dipol momenti: 1,15 debay
- Dielektrik keçiriciliyi: 4,806 20 °C
Kimyəvi xassələri
redaktəSu ilə azeotrop qarışıq əmələ gətirir (qaynama T. 56,2 °C, 97,4 % xloroform)
Alınması
redaktəXloroform sənayedə metanın və ya xlormetanın xlorlaşması yolu ilə istehsal edilir. Reaksiyanı 400 – 500 °C temperaturda aparırlar. Bu zaman bir sıra kimyəvi reaksiyalar gedir. Bu cür reaksiyalar ultrabənövşəyi şuaların təsiri ilə də gedir:
- CH4+ Cl2 → CH3Cl + HCl
- CH3Cl + Cl2 → CH2Cl2 + HCl
- CH2Cl2 + Cl2 → CHCl3 + HCl
- CHCl3 + Cl2 → CCl4 +HCl
Nəticədə metilxlorid, dixlormetan, xloroform və tetraxlormetan qarışığı alınır. Qarışıqdan birləşmələr distillə yolu ilə ayrılır. Xloroformu laboratoriyada aseton və ya etanolu əhəng məhlulu ilə işləməklə alırlar. Satışa çıxarılan xloroformu oksigen təsirindən uzun müddət qorumaq üçün stabilizator kimi 1-2% etil spirti qarışdırılır. Xloroform Beylşteyn reaksiyasında tətbiq olunur:
- 5CuO + 2CHCl3 → 3CuCl3 + 2CO2 + H2O + 2Cu
Tətbiqi
redaktəXloroform XIX əsrin axırı və XX əsrin əvvəllərində cərrahiyyə əməliyatları zamanı anestetik maddə kimi istifadə olunmuşdur. Xloroform cərrahi əməliyyatlar zamanı narkoz vasitəsi kimi ilk dəfə şotlandlı həkim Simpson tərəfindən 1848-ci ildə istifadə edilmişdir. Xloroform Rusiyada narkoz vasitəsi kimi ilk dəfə olaraq N.İ.Piroqov tərəfindən istifadə olunub. Lakin sonralar daha təhlükəsiz maddələrlə əvəz edilib.
Xloroform xlordiftormetanın – freonun (xladon-22) istehsalında istifadə olunur. Freon xloroforma sürmə(V) xloridin iştirakı ilə hidrogen ftoridlə təsir etməklə Svarts reaksiyası üzrə alırlar:
- CHCl3 + 2HF □(→┴(SbCl_5 ) ) CF2HCl + 2HCl
Xloroform həmçinin farmakologiya sənayesində, o cümlədən boya maddələrinin və pestisidlərin istehsalında həlledici qismində istifadə olunur. Deyterium tərkibli xloroform (CDCl3) nüvə maqnit rezonansı (NMR) üçün ümumi həlledici kimi istifadə olunur.
Təmizləmə
redaktəTəmizləmə bir neçə mərhələdə aparılır. İlk növbədə xloroformu qatı sulfat turşusu ilə çalxalayır sonra kalsium xlorid və ya maqnezium sulfat üzərində qurudur və qovurlar. Xloroformun təmizliyini yoxlamaq üçün süzgəc kağızı üzərində buxarlandırırlar: xloroform uçduqdan sonra süzgəc kağızında iy qalmamalıdır. Süzgəc kağızından kəskin və ya qıcıqlandırıcı iy gələrsə, bu hal xloroformda hidrogenxlorid və ya fosgen qarışığı qaldığını göstərir.
Orqanizmə təsiri
redaktəXloroformla nəfəs almaq mərkəzi sinir sisteminə pis təsir edir. Nəfəs alarkən havada xloroformun miqdarı 0,09% olduqda qısa müddət ərzində başgicəllənmə, yorğunluq və baş ağrısı halları yaranır. Xloroformla daima əlaqədə olduqda qaraciyər və böyrək xəstəlikləri yarana bilər. Yer kürəsi əhalisinin təqribən 10%-nin xloroforma qarşı allergiyası var. Çox hallarda insanlarda (təqribən 70-80%) öyümə halları olur. Heyvanlar üzərində aparılan təcrübələr nəticəsində müəyyən edilmişdir ki, bala gözləyən siçovul tərkibində 0,003% xloroform olan hava ilə nəfəs aldığı halda balasını vaxtından əvvəl itirmiş olur. Müəyyən edilmişdir bu cür şəraitdə nəfəs alan siçovul və siçanların həyata gətirdiyi balaları qüsurlu olur. Xloroformun insan artımına təsiri yaxşı öyrənilmişdir. Xloroformla uzun müddət nəfəs yolları və selikli qişa ilə qarşılıqlı təsirdə olan insanlarda ölüm halları baş verə bilər. Bu hal yalnız havada xloroformun qatılığının artması nəticəsində baş verir. Xloroform orqanizmə düşdükdə dərhal havaya çıxmaq tələb olunur. Xloroform orqanizmdə qalması karbon oksidinin və hidrogenxloridin4 yaranmasına şərait yaradır.
- 2CHCl3 + 2H2O + O2→ 2CO2 ↑ + 6HCl↑
Xloroform kifayət qədər saxlanarsa onun oksigenlə qarşılıqlı təsiri zamanı fosgen alınır: 2CHCl3+ O2 → 2COCl2↑ + 2HCl ↑
Mənbə
redaktə- http://www.cdc.gov/niosh/npg/npgd0127.html
- Хлороформ ⌬ органические растворители на Chemical Region
- Промышленные фторорганические продукты: справочное издание / Б.Н. Максимов, В.Г. Барабанов, И.Л. Серушкин и др.. — 2-е, перераб. и доп.. — СПб: «Химия», 1996. — 544 с. — ISBN 5-7245-1043-X.
- В. Ф. Крамаренко. Токсикологическая химия. — К.: Выща шк., 1989. — 447 с. — 6 000 экз. — ISBN 5-11-000148-0.