Natrium tiosulfat
Natrium tiosulfat (antixlorin, hiposulfit, natrium sulfidotrioxosulfate, natrium sulfat) — qeyri-üzvi birləşmə, Na2S2O3 və ya Na2SO3S kimyəvi formulu ilə natrium və tiosulfurik turşunun duzudur, Na2S2O3 5H2O tərkibli kristal hidrat yaradır. Tibbdə, fotoqrafiyada və digər sahələrdə istifadə olunur.
| Natrium tiosulfat | |
|---|---|
 | |
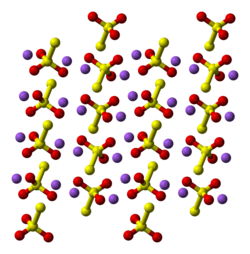 | |
 | |
| Ümumi | |
| Ənənəvi adı | hiposulfit |
| Kimyəvi formulu |
Na2S2O3 Na2S2O3·5H2O (kristal hidrat) |
| Molyar kütlə | 248,17 q/mol |
| Fiziki xassələri | |
| Aqreqat halı (n.ş.) | qoxusuz ağ kristallar |
| Sıxlıq | 1.667 q/sm3 q/sm³ |
| Termik xüsusiyyətlər | |
| Ərimə nöqtəsi | 48,5 °С (pentahidrat) °S |
| Qaynama nöqtəsi | 100 °S |
| Kimyəvi xassələri | |
| Suda həllolma | 70,120; 22980 q/100 ml |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 7772-98-7 |
| PubChem | 24477, 60054324, 168014062 |
| SMILES | [Na+].[Na+].[O-]S([O-])(=O)=S |
| RTECS | XN6476000 |
| ChEBI | 132112 |
| ChemSpider | 22885 |
| Toksikologiya | |
| Zəhərliliyi | |
Tarixi arayışı
redaktəNatrium tiosulfat, ehtimal ki, ilk dəfə 1799-cu ildə natrium sulfatı kömürlə qızdıran Fransua Şosse tərəfindən əldə edilmişdir. 1877-ci ildə Vaqner, müvafiq turşu üçün "tiosulfurik" adını tövsiyə etdi, bundan sonra "natrium tiosulfat" termini kimyəvi ədəbiyyatdan əvvəlki adı "natrium hiposulfit" i demək olar ki, tamamilə əvəz etdi.[1] Yodun titrlənməsi üçün bir reaktiv kimi natrium tiosulfat 1853-cü ildə Şvarts tərəfindən təklif edilmişdir (Karl Leonard Henrix Şvarts, 1824-1890).[2]
Alınması
redaktə- sodium polisulfidlərin oksidləşməsi;
- artıq kükürdün Na2SO3 ilə qaynadılması:
- H2S və SO2-nin NaOH ilə qarşılıqlı təsiri (NaHSO3, kükürd boyaları istehsalında, sənaye qazlarının S-dən təmizlənməsində yan məhsul):
- natrium hidroksid ilə artıq kükürdün qaynadılması:
sonra, yuxarıdakı reaksiyaya görə natrium sulfitə sodium tiosulfat yaratmaq üçün kükürd əlavə edir. Eyni zamanda, bu reaksiya zamanı natrium polisülfidlər əmələ gəlir (məhlula sarı rəng verirlər). Onları məhv etmək üçün SO2 məhlulu qatılır.
- saf susuz natrium tiosulfat kükürdün formamiddə natrium nitritlə reaksiya verilməsi ilə əldə edilə bilər. Bu reaksiya kəmiyyət olaraq (30 dəqiqə ərzində 80 ° C-də) tənliyə görə davam edir:
- natrium sulfidin atmosferdə oksigen iştirakı ilə suda həll edilməsi:
Fiziki və kimyəvi xüsusiyyətləri
redaktəGörünüşcə rəngsiz kristallardır. Üç dəyişiklik yaradır: monoklinik α (a = 0.8513, b = 0.8158, c = 0.6425, β = 97.08 °, z = 4, kosmik qrup P21 / c), həmçinin β və γ. α-modifikasiya 330 ° C-də β, 80 380 ° C-də γ-ə çevrilir. Α-modifikasiyanın sıxlığı 2,345 q / sm3-dir.[3]
Suda həll olunur (50.1 g / 100 ml (0 ° C), 70.2 q / 100 ml (20 ° C), 231.8 q / 100 ml (80 ° C)).[3]
Molyar kütlə 248,17 q / mol (pentahidrat). 48.5 ° C-də kristal hidrat kristallaşma suyunda həll olur və çox doymuş məhlul əmələ gətirir; təxminən 100 ° C-də susuzlaşır.
220 ° C-yə qədər qızdırıldıqda, sxemə görə parçalanır:
Natrium tiosulfat güclü açıcı vasitədir:
Güclü oksidləşdirici maddələrlə, məsələn sərbəst xlorla, sulfatlara və ya kükürd turşusuna qədər oksidləşir:
Zəif və ya daha yavaş fəaliyyət göstərən oksidləşdirici maddələr, məsələn, yod, tetrationik turşu duzlarına çevrilir:
Bu reaksiya çox vacibdir, çünki yodametriya üçün əsas rol oynayır. Qeyd etmək lazımdır ki, bir qələvi mühitdə natrium tiosulfatın yod ilə oksidləşməsi sulfata qədər davam edə bilər.
Natrium tiosulfatın güclü turşu ilə reaksiyası ilə tiosulfurik turşunu (hidrogen tiosulfat) təcrid etmək mümkün deyil, çünki qeyri-sabitdir və dərhal su, kükürd və kükürd dioksidə çevrilir:
Eritilmiş kristal hidrat Na2S2O3 · 5H2O hipotermiyaya çox meyllidir.
Tətbiqi
redaktə- parçaların ağarmasına səbəb xlor izlərini aradan qaldırmaqda;
- filizlərdən gümüş çıxarmaq üçün;
- fotoqrafiyada fiksator; [4]
- iyodometriyada reaktiv;
- zəhərlənmə üçün antidot: As, Br, Hg və digər ağır metallar, sionidlər (onları tiosionatlara çevirir) və s .;
- bağırsaq dezinfeksiyası üçün;
- qoturun müalicəsi üçün (xlorid turşusu ilə birlikdə);
- antiinflamatuar və yanıq əleyhinə vasitə;
- donma nöqtəsini endirərək molekulyar ağırlıqların təyin edilməsi üçün vasitədir (krioskopik sabit 4.26 °);
- qida sənayesində qida qatqısı E539 olaraq qeydiyyata alınmışdır;
- beton əlavələri;
- toxumaları yoddan təmizləmək;
- natrium tiosulfat məhlulu ilə isladılmış cuna sarğıları tənəffüs sistemini zəhərli maddə xlordan Birinci Dünya müharibəsində qorumaq üçün istifadə edilmişdir;
- lidokainin yüksək dozası üçün antidot.
Həmçinin bax
redaktəİstinadlar
redaktəƏdəbiyyat
redaktə- // Энциклопедический словарь Брокгауза и Ефрона: В 86 томах (82 т. и 4 доп.). СПб.. 1890–1907.
- Петрашень, Владимир Иванович. Объемный анализ. М.—Л.: Госхимиздат. 1946.
- Гурлев Д. С. Справочник по фотографии (обработка фотоматериалов). К.: Тэхника. 1988.
- Куликова Л. Н. Натрия тиосульфат. 3.
