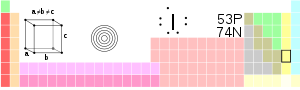
Yod
Bu məqalədəki məlumatların yoxlanıla bilməsi üçün əlavə mənbələrə ehtiyac var. |
Bu məqaləni vikiləşdirmək lazımdır. |
| ||||||
| Ümumi | ||||||
|---|---|---|---|---|---|---|
| Ad, İşarə, Nömrə | 《yod》, I, 53 | |||||
| Qrup, Dövr, Blok | 17, 5, p | |||||
| Xarici görünüşü | 
| |||||
| Atom kütləsi | 126.90447 q/mol | |||||
| Elektron formulu | [Kr] 4d10 5s2 5p5 | |||||
| Fiziki xassələr | ||||||
| Halı | ||||||
| Sıxlığı | (0 °C, 101.325 kPa) q/L | |||||
| Ərimə temperaturu | 113.7 °C (386.85 K, 236.66 °F) | |||||
| Qaynama temperaturu | 184.3 °C (457.4 K, 363.7 °F) | |||||
| Elektromənfiliyi | ||||||
| Oksidləşmə dərəcəsi | ||||||
| Spektr = | ||||||
| İonlaşma enerjisi | kCmol-1 | |||||
Yod (I) — D. İ. Mendeleyevin elementlərin dövri sistemində 53-cü element.
Etimologiya
redaktəBənövşəyi buxarlarına görə yod sözü qədim yunan dilində mənası bənövşəyi olan iodes sözündən götürülmüşdür.[1]
Ətraflı məlumat
redaktəYod (I) – 70 kq ağırlığında sağlam insanın orqanizmində təxminən 25 mq-dır. Bir gün ərzində qalxanabənzər vəzidən qana 100–300 mkq-a qədər hormonal yod keçir. İnsan qidasında yodun çatışmazlığı endemik ur (zob) xəstəliyinin əmələ gəlməsinə səbəb olur. Yod balıqda (5–8 mkq%), dəniz suyunda, feyxoada (390 mkq%), dəniz kələmində, balıq yağında vardır.
Suyunda yod çatışmayan rayonların əhalisi üçün yodlaşdırılmış duz hazırlanır. 1 ton duza 25 q KJ əlavə edilir ki, həmin duz vasitəsilə insan sutkada 200 mkq yod qəbul edir. Sutkalıq tələbat insanın əməyindən və həyat tərzindən asılı olaraq 100–260 mkq-dır. Mikroelementlər yeyinti məhsullarında cüzi miqdarda vardır və bunların miqdarı mikroqram və ya qamma ilə göstərilir. Mikroelementlərin də orqanizm üçün çox böyük əhəmiyyəti vardır. Belə ki, Cu və Co qanın əmələ gəlməsində, F və Mn dişlərin formalaşmasında iştirak edir. Yod davamlı hallogenlərin ən ağırıdır. Adi şəraitlərdə dörd hallogendən yalnız yod bərk bəsit maddə kimi mövcuddur. Bu demək olar ki, zəif metallik parıltılı və bənövşəyi çalarlı qara kristallardır. Əgər yod kristalları sınaq şüşəsinin dibində yerləşirsə, onda onun üzərində hava zəif bənövşəyi rəng alır. Qızdırdıqda kristallar tamamilə sublimasiya olunur və intensiv bənövşəyi buxarlar əmələ gətirir.
Təbiətdə yod nadir və səpələnmiş elementdir, amma canlı sistemlər onu dəfələrlə qatılaşdıra bilər. Belə xassə laminariya yosununda kəskin ifadə olnur. Bir ton dəniz suyunda 20–30 mq yod olur, bir ton qurudulmuş laminariyada 5 kq-a qədər yod olur. Bu qədər yod 200 min ton dəniz suyunda ola bilər, amma sahilə çıxan yosunlarda yod oksigen ilə oksidləşir və havada yod iyi hiss olunur. Beləliklə, yod yeganə hallogendir ki, biosferdə təbii proseslər nəticəsində sərbəst halda əmələ gəlir. Yod biogen mikroelementdir. İnsan orqanizmində normal həyat fəaliyyəti üçün 13 mq-a qədər yod olmalıdır. Bu kütlənin yarıya qədəri qalxanabənzər vəzdə toplanır (qalxanabənzər vəzin kütləsi cəmi 20 qramdır). Asanlıqla hesablamaq olar ki, qalxanabənzər vəzdə yodun miqdarı digər orqanlarda və toxumalarda olduğundan təxminən 3000 dəfə çoxdur.
Yod analitik kimyada istifadə üçün ən qiymətli oksidləşdiricidir. Amma o xüsusi xassəyə malik olmasaydı bu mümkün olmazdı: J2 molekulu J– ionuna birləşərək J3– kompleksi əmələ gətirir. Bu zaman yodun oksidləşdirici xassəsi praktiki olaraq dəyişmir, həll olma kifayət qədər artır ki, bu da analitik praktika üçün məhlul hazırlamağa imkan verir.
Yod yüksək təmizlikli metalları almaq üçün nəqliyat reaksiyalarında xüsusi tətbiq tapdı. Bu üsulun əsasında yodun aktivliyinin onun birləşmələrinin termiki davamsızlığı arasındakı uğurlu əlaqə durur. Sirkoniumun təmizlənməsi misalında üsulun mahiyyətinə baxaq. Qarışıqlardan təmizlənməli olan metal və yod vakuum kamerasına qoyulur ki, onun içərisinə təmiz metaldan keçirici bərkidilir. Bütün kamera içindəki ilə birlikdə qızdırılır, keçirici isə elektrik cərəyanı ilə közərdilir. Yod sirkonium ilə reaksiyaya girərək uçucu sirkonium (IV) yodid əmələ gətirir:
Zr + 2J2 ↔ ZrJ4
Közərmiş keçirici səthində sirkonium (IV) yodid əks reaksiya ilə parçalanır və yüksək təmizlikli metalın kristalları böyüməyə başlayır.
Yod ən az üzvi maddələrin izlərinin yaxşı əks etdiricisidir.[2]
Tarixi
redaktəBernard Courtois barut istehsalında istifadə edilməsi üçün Kalium-Nitrat istehsal edən Jean-Baptiste Courtois-in oğlu idi. Courtois kimya təhsili aldı və hərbi xəstəxanalarda əczaçı olaraq çalışdı. Atası borc səbəbiylə həbsə girincə, Courtois Kalium-Nitrat işinə girdi. Napaleonun ordularına barut düzəltmək üçün lazım olan Kalium-Nitrat (Hindistan Şorası) Fransada istehsal edilirdi. Courtois kalium-karbonatı dəniz yosunu küllərindən əldə edirdi. Şumerlər və Misirlilər dəniz küllərini sabun yerinə istifadə bilirdi. Kalium karbonat kiri təmizlədiyi üçün Afrikada hələ də sabun yerinə bu külü istifadə edən qəbilələr vardır. Courtois dəniz yosunu külündəki kalium-karbonatı külləri suyla yuyaraq təcrid etməkdə idi. Küllərə sulfat turşusu töküb istənməyən maddələri də uzaqlaşdırırdı. Courtois 1811-ci ildə bir gün sulfat turşusu çox tökdükdə qarışıqdan bənövşəyi bir qaz çıxdı. Bənövşəyi rəngli qaz soyuq bir səthə vuran tünd rəngli kristallara çevrilmişdi. Bu maddənin nə olduğunu anlamaq istəyən Courtois kristalları yığdı. Kristalların bəzilərini araşdırması üçün qazlar mövzusunda mütəxəssis olan kimyaçı Jozef Lui Gey-Lüssaka, bəzilərini də fizik Andre Mari Amperə verdi. Gey-Lüssak bunun yeni bir element ola biləcəyini açıqladı və maddəyə "iode" adını verdi. AMPS, kristalların bəzilərini İngilis kimyaçı H.Davy'ye vermişdi. Davy, yodun yeni bir element olduğunu kəşf etdiyini elan edincə Gey-Lüssak ilə aralarında anlaşılmazlıq çıxdı. Ancaq hər ikisi də yod adlı elementi ilk dəfə Courtois’in təcrid ettiyini açıqladı.[3]
Yod məhlulu və indiki vaxtda istifadə edilən Batikonun tərkibini Yod təşkil edir.
İstinadlar
redaktə- ↑ "Atomic Weight of Iodine | Commission on Isotopic Abundances and Atomic Weights". www.ciaaw.org. 2024-08-21 tarixində arxivləşdirilib. İstifadə tarixi: 2024-09-22.
- ↑ Musayev N. Х. "Ərzaq malları əmtəəşünaslığının nəzəri əsasları". Dərslik. Bakı, "Çaşıoğlu" nəşriyyatı, 2003 – 368 səh.
- ↑ Wisniak, Jaime. (2002). Bernard Courtois – The Discoverer of Iodine. Educación Química. 13. 206-213. 10.22201/fq.18708404e.2002.3.66295.
Xarici keçidlər
redaktə Kimya haqqında olan bu məqalə bu məqalə qaralama halındadır. Məqaləni redaktə edərək Vikipediyanı zənginləşdirin. |